O przenoszeniu elektronów dalekiego zasięgu w „PNAS”
-
Nadrzędna kategoria: Wiadomości Naukowe
Badacze z Instytutu Chemii Organicznej PAN, Uniwersytetu Kalifornijskiego i Kalifornijskiego Instytutu Technicznego odkryli, w jaki sposób może zachodzić przeniesienie elektronów dalekiego zasięgu. Opis badania publikuje „PNAS”. To pierwszy artykuł naukowców IChO PAN, który ukazał się w tym periodyku.
Prof. Daniel Gryko ze współpracownikami z ICHO PAN (prof. Agnieszką Szumną, dr Olgą Staszewską-Krajewską, dr Hanną Jędrzejewską) oraz z Kalifornii (prof. Harrym Gray’em, prof. Valentine Vullev) odkrył, w jaki sposób może zachodzić przeniesienie elektronów dalekiego zasięgu. Pierwszym autorem pracy jest Rafał Orłowski z IChO PAN. Odkrycie zostało opublikowane w prestiżowym „Proceedings of the National Academy of Sciences of the USA” (PNAS).
Przeniesienie elektronów dalekiego zasięgu przenika biologię, chemię i inżynierię, ponieważ ma kluczowe znaczenie dla procesów podtrzymujących życie, przemian chemicznych, konwersji energii, systemów elektronicznych i technologii fotonicznych. Wyjaśnienie, co rządzi szybkością przeniesienia elektronów, ma nie tylko ogromne znaczenie dla zrozumienia przepływu energii w biologii, ale może być też pomocne w projektowaniu i konstruowaniu urządzeń elektronicznych.
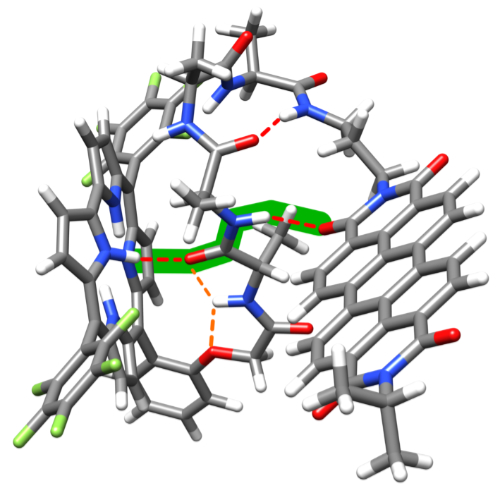
Prof. Gryko ze współpracownikami odkrył ultraszybkie przeniesienie elektronów (ET) od donora do akceptora, połączonych układem 20 wiązań kowalencyjnych. Chociaż takie duże odległości pomiędzy chromoforami uniemożliwiają ET, uczeni zaobserwowali pikosekundowe procesy ET z ilościowymi wydajnościami kwantowymi, na których kinetykę nie ma większego wpływu zmniejszanie liczby aminokwasów w łączniku. Połączenie NMR, dichroizmu kołowego i obliczeń kwantowo-mechanicznych ujawnia, że wewnątrzcząsteczkowe wiązania wodorowe zbliżają do siebie donor (korol) i akceptor (perylenodiimid) w architekturze molekularnej „w kształcie skorpiona”, umożliwiając w ten sposób przeniesienie elektronów. Ten rewolucyjny rezultat pokazuje, że krótkie peptydy, zawierające zaledwie cztery reszty aminokwasowe, zapewniają sieć wiązań wodorowych, która może pośredniczyć w przenoszeniu elektronów z niezwykle wysoką wydajnością. Praca ta nie tylko zmienia spojrzenie na projektowanie cząsteczek, w których zachodzi przeniesienie elektronu, ale także sugeruje motywy strukturalne pośredniczące w ET w białkach.
Treść artykułu „Role of intramolecular hydrogen bonds in promoting electron flow through amino acid and oligopeptide conjugates” w „PNAS” https://doi.org/10.1073/pnas.2026462118
Źródło informacji: Instytut Chemii Organicznej PAN
